 |
Autor: Dr. Carlos Tajer.
Un polémico artículo que pone en tela de
juicio nuestras creencias sobre el tema de la obesidad. Reflexiones
inteligentes y a menudo contraintuitivas que no lo dejarán indifierente.
Comentario de la Dra. Mónica Katz que expresa una posición contraria.
¡Lo invitamos a opinar! |
Dr. Carlos Tajer.Revista SAC
Introducción
Creer que comprendemos nuestro mundo
tiene efectos placenteros y sedantes. La creatividad puesta en la
interpretación de fenómenos de difícil explicación, como el origen del
universo, o “simplemente” la salida del sol o las fases de la luna,
contribuyeron en cada período histórico y cultura a configurar modelos,
mitológicos o científicos, que aportaban una visión abarcadora de la
realidad. Las religiones y hoy la ciencia para una parte de la población
cumplen esa función: son interpretaciones comprensivas de una realidad
compleja, que nos permiten transcurrir por nuestra vida con mayores
certezas.
También en medicina elaboramos teorías que nos ayudan a enfocar
globalmente problemas de salud y adoptar decisiones frente a pacientes
individuales. Necesitamos verdades sencillas que consoliden nuestro
pensamiento operativo. Cuando aspectos de nuestra experiencia o de la
realidad explorada no cierran en ese modelo, solemos adoptar, tanto en
forma individual como comunitaria, dos actitudes que habitualmente
coexisten: la primera reacción es ignorar o negar el fenómeno, y cuando
la negación es ya imposible, buscar un nuevo modelo explicativo.
Algo así está ocurriendo con nuestra concepción del peso corporal ideal y la dieta.
El peso corporal, la masa muscular, su componente graso y su
distribución aparecen simplificadas bajo el concepto de “normalidad” y
obesidad. En forma similar al modelo del colesterol y la presión
arterial, pensamos al peso corporal con la ecuación” cuanto más, peor” y
pretendemos determinar así a un hipotético peso ideal.
No tenemos duda de que el aumento de peso se asocia al desarrollo de
hipertensión arterial, diabetes y enfermedades cardiovasculares, además
de múltiples disturbios metabólicos y otros males. Por ese motivo se
han buscado criterios de corte para definir niveles de peso como
normales, excesos y obesidades de diferente grado y facilitar las
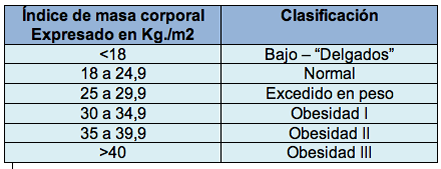
conductas.La definición habitual utiliza el índice de masa corporal
(IMC) (en inglés, body mass index - BMI), que se obtiene de dividir el
peso en kilogramos por la altura expresada en metros elevada al
cuadrado. Así, una persona de 75 kg y 1,60 m de estatura tiene un IMC o
BMI de 29,3. Tabla 1.
La asociación con el riesgo cardiovascular se verifica también con
otros marcadores de obesidad, como el índice cintura cadera (ICC) o el
perímetro de la cintura, lo que discutiremos más adelante.
Tabla 1
Categorización de niveles de obesidad de acuerdo al índice de masa corporal
Dentro de esta concepción produce un impacto perturbador el hallazgo de que en diferentes contextos de enfermedad, los
pacientes con “exceso de peso” u “obesidad moderada grado I” cursan con
menos riesgo de muerte y nuevos eventos cardiovasculares que los
“normales” y los delgados. La aparente protección de la obesidad se
observa en seguimientos luego de un evento o intervención coronaria
(posinfarto, angioplastia, cirugía de revascularización), en la
insuficiencia cardíaca crónica y luego de un accidente cerebrovascular.
Este fenómeno se ha denominado la paradoja de la obesidad.
Este artículo estará dedicado a explorar
lo que conocemos sobre “obesidad” en prevención secundaria, con el
objetivo de reiterar una información muy rica y sistemáticamente
ignorada, y contribuir a reflexionar sobre la racionalidad de las
conductas y el discurso frente a los pacientes.
Las curvas de riesgo y la paradoja de la obesidad
La mayor revisión del tema consideró 40 estudios que abarcaron 250.152 pacientes con enfermedad coronaria seguidos a 3,8 años.1 Construyeron
para el análisis curvas de la relación entre el IMC y la mortalidad en
el seguimiento corregido para múltiples covariables. Tomando como grupo
control a los denominados normales, los pacientes delgados con IMC <
18 kg/m2 tuvieron un incremento de la mortalidad global y
cardiovascular. Los pacientes con sobrepeso 25 a 29,9 de IMC tuvieron
menor riesgo que los normales. Los pacientes obesos 30-35 de IMC
tendieron a un menor riesgo de mortalidad global o cardiovascular, y aún
en el grupo con obesidad severa, >=35 de IMC, no se observó aumento
de la mortalidad global.
Resumo: El mayor riesgo lo tienen las personas delgadas, luego
siguen los normales y muy obesos, y los grupos de mejor evolución son
los de exceso de peso y obesidad moderada.
El lector pensará que estoy cometiendo un error o que hay algo raro en
esta información. Transcribiré los gráficos y comenzaremos con su
descripción. Figura 1.
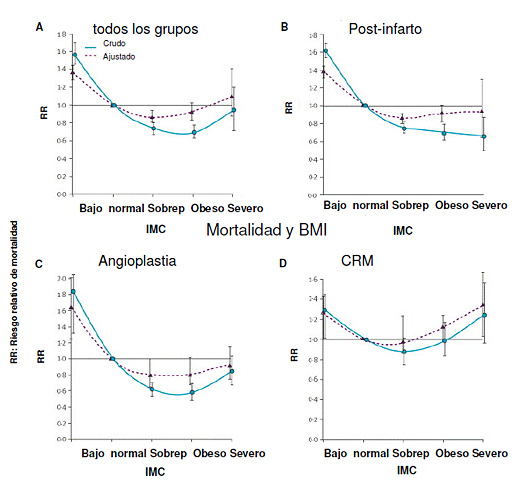 Relación entre las categorías de
peso utilizadas en la tabla I y el riesgo de muerte de cualquier causa
en 3,8 años de seguimiento en más de 250.00 pacientes con
coronariopatía. Como Riesgo relativo 1 se consideró al grupo normal (IMC
18 a 24,9 kg/m2). En línea continua se expresa el riesgo crudo y con
línea punteada el ajustado por edad. Modificado de cita 1.
Relación entre las categorías de
peso utilizadas en la tabla I y el riesgo de muerte de cualquier causa
en 3,8 años de seguimiento en más de 250.00 pacientes con
coronariopatía. Como Riesgo relativo 1 se consideró al grupo normal (IMC
18 a 24,9 kg/m2). En línea continua se expresa el riesgo crudo y con
línea punteada el ajustado por edad. Modificado de cita 1.
En la figura 1, que considera a
todos los pacientes en conjunto, se observa que tomando como índice de
riesgo 1 al IMC normal (>18 y <25), el riesgo relativo de los
delgados fue 1,6 (es decir tenían un riesgo 60% mayor), El riesgo
disminuía respecto de los normales en los pacientes con sobrepeso y los
obesos. Los denominados obesos severos alcanzaban el mismo riesgo que
los “normales”. Este fenómeno no es homogéneo, y se acentúa en los
pacientes posinfarto y posangioplastia. Luego de una angioplastia,
cualquiera fuera el grado de obesidad, ¡la tendencia es a menor riesgo aún en los obesos que en los normales!
Mirando estas curvas, que incluyen todas las grandes
series hasta el 2006 y se repiten en las posteriores, no cabe duda que
el mayor riesgo evolutivo en prevención secundaria se concentra en los
pacientes delgados, y el segundo grupo de riesgo es el grupo con IMC
“normal”.
Un fenómeno similar se ha observado en otras patologías. Por ejemplo en
pacientes luego de un accidente cerebrovascular isquémico, en un
estudio con 20.246 casos, con un seguimiento a 2,5 años. El riesgo
ajustado de un nuevo evento vascular fue 14% menor en los pacientes con
sobrepeso y 16% menor en los obesos , en comparación con los normales o
delgados.
Esta observación es contra-intuitiva; sólo comentar en una recorrida de
unidad coronaria que el pronóstico de este paciente a largo plazo
preocupa porque es delgado, induce miradas incrédulas e incluso
compasivas. Es curioso comprobar cómo lo que no se entiende en medicina o
no puede incorporarse a un cuerpo coherente de ideas simplemente se
hace invisible o inexistente.
La paradoja de la obesidad pone en cuestionamiento las recomendaciones
dietéticas y de reducción de peso en pacientes con enfermedad
cardiovascular, y han generado un debate activo intentando comprender el
mensaje implícito.
Repasaremos las principales hipótesis explicativas de esta observación,
para luego discutir en qué medida estos hallazgos pueden influenciar las
conductas frente al paciente individual.
Buscando una explicación a la paradoja en enfermedad coronaria
Explicación 1: Inadecuada comprensión de factores confundidores
El fenómeno de los factores de riesgo y la mortalidad aguda del infarto
La epidemiología nos enseña que asociación entre variables no indica
causalidad ni mecanismos. Por ejemplo hace unos años se discutió mucho
la implicación del tabaquismo en la evolución aguda y alejada del
infarto. Se observó que los pacientes tabaquistas que se infartaban,
tenían una menor mortalidad intrahospitalaria.
Este dato generó una confusión con el rol del tabaco: ¿cómo un factor de
riesgo tan documentado y agresivo podía en otro plano ser protector?
Analizando con mayor profundidad se detectó una variable confundidora
muy fuerte, la edad. Las personas que se infartan fumando tienen 10 a 15
años menos que los no fumadores. Dado que la mortalidad del infarto
guarda relación con la edad, al corregir estadísticamente para cada
grupo etario, el tabaco perdía su rol “protector” durante la fase aguda.
Este fenómeno paradójico del tabaco sobre la evolución aguda, se
reproduce también para el índice de masa corporal y todos los restantes
factores de riesgo, en forma muy curiosa. En un estudio reciente, la
mortalidad durante la etapa hospitalaria era menor cuanto mayor fue el
número de factores de riesgo, considerando al antecedente de
hipertensión, dislipemia, tabaquismo, diabetes e historia familiar de
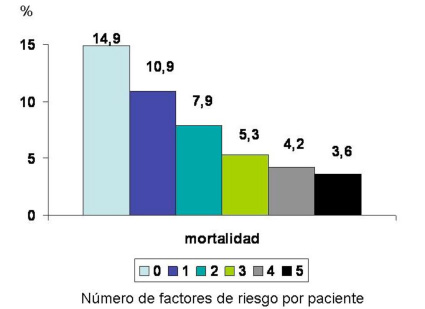
enfermedad coronaria3 .Como se
ve en la figura 2, la mortalidad fue cuatro veces mayor en los pacientes
sin factores de riesgo (14,9%) que en los que tenían los cinco
considerados (3,6%). La mejor explicación para esta aparente paradoja es
que los factores de riesgo adelantan la aparición de enfermedad
coronaria, y que el infarto internado tiene mayor mortalidad con la
edad. De hecho existieron 14 años de diferencia en la edad promedio de
los pacientes sin ningún factor de riesgo, 71,9 años, frente a 56,8 años
con 5 factores. Corrigiendo por edad y otras variables, el riesgo
relativo entre ambos ya no es de 4 veces sino 1,6, es decir, un 60%
mayor. Se sospecha la presencia de otras variables no consideradas en el
modelo, es decir, otros “confundidores” además de la edad o los
considerados en el análisis que podrían explicar la observación.
El mismo fenómeno ocurre con el índice de masa corporal y la evolución
en agudo: los pacientes más delgados tienen mucha mayor edad que los de
mayor peso y la explicación en este sentido podría ser simplemente la
existencia de variados factores confundidores no reconocidos. Esta
explicación, que funciona muy bien para la evolución aguda, ¿será la
solución del enigma de la paradoja de la obesidad en el seguimiento
alejado?
Figura 2
Relación
entre en número de factores de riesgo como antecedente y el riesgo de
muerte durante la etapa hospitalaria en 542.008 pacientes del National
Registry of Myocardial infarction. Canto et al (3).
El control de los factores de riesgo y la mortalidad alejada luego de un infarto
El problema de los factores de riesgo y su influencia en el
seguimiento alejado es bastante diferente. Luego de un infarto, se
transforma cuando consideramos el seguimiento luego del infarto. Las
personas que siguen fumando, mantienen elevados el colesterol ó la
presión arterial, incrementan el riesgo en el seguimiento, es decir,
estos factores siguen implicando riesgo de una peor evolución alejada si
no son corregidos.
En el tema del índice de masa corporal y obesidad el rol de los
confundidores, y en particular la edad, puede ser una buena explicación
para la evolución aguda, pero no es suficiente para explicar la
evolución alejada por lo menos conceptualmente. No tenemos un
tratamiento validado para inducir una reducción de peso estable tanto en
prevención primaria como secundaria, y habitualmente el IMC no se
modifica en el seguimiento en las series, a diferencia de los factores
de riesgo habituales. A pesar de que el IMC no se modifica el riesgo
evolutivo es menor cuanto mayor el peso e IMC inicial.
En la práctica clínica es muy difícil lograr una reducción estable del
peso, lo que puede ilustrarse con los resultados del estudio Courage 4.
El ensayo incluyó 2287 pacientes coronarios crónicos para evaluar el
rol de la angioplastia bajo un óptimo tratamiento médico. Respecto a los
valores basales, que eran bastante aceptables, lograron reducciones muy
importantes de los niveles de colesterol, presión arterial, y
tabaquismo que se mantuvieron en los cinco años de seguimiento. Pudieron
inducir asimismo un incremento de las horas de ejercicio semanal y
cambios en el estilo de dieta, pero no tuvieron efecto sobre el peso
corporal. El Índice de masa corporal inicial de 28,7±0,18 kg/m2
aumentó levemente a 29.0±0.21 kg/m2 a los cinco años tanto en los
pacientes angioplastiados con tratamiento médico. Los cardiólogos
reconocerán que esto se asemeja mucho a la observación cotidiana del
consultorio sobre lo que podemos lograr o no en nuestros pacientes.
A pesar de los múltiples tratamientos estadísticos, la relación
paradójica entre el índice de masa corporal y la mortalidad no ha podido
ser corregida por factores confundidores.
Explicación 2: El índice de masa corporal no es un buen discriminador del porcentaje de peso graso.
En la revisión de Canto y col.3
comentada anteriormente, los autores escribieron como conclusión del
estudio: “La mejor evolución de la mortalidad cardiovascular y total
observada en pacientes con sobrepeso u obesos moderados no puede ser
explicada por el ajuste con factores confundidores. Estos hallazgos
pueden ser explicados por la falta de poder discriminatorio del Índice
de masa corporal para diferenciar entre la grasa corporal y la masa
magra.”.
Esta hipótesis es muy interesante: hay personas con mayor peso a
expensas de masa muscular y otros con menor peso pero una mayor
proporción de peso graso. Hipotéticamente, la proporción de peso graso
contendría el mensaje de riesgo.
En diversas series epidemiológicas en población sana surge sustento para
este argumento. En un estudio observaron en 787 varones con seguimiento
a 22 años un comportamiento en J de acuerdo al IMC5. Calcularon
también el porcentaje de peso graso y la masa magra, y con esa
corrección, desapareció la J: el riesgo fue linealmente mayor a mayor
porcentaje de masa grasa. Divididos por quintilos, el quintilo de mayor
porcentaje de peso graso tuvo una mortalidad 40% superior al quintilo
más bajo.
Sin embargo esta no parece ser la explicación en pacientes coronarios, y
fue refutada por un minucioso estudio prospectivo en el cual se estimó
el porcentaje de grasa corporal con mediciones de los pliegues cutáneos y
su distribución6. En esa
serie definieron alta composición de grasa corporal cuando era >25%
en hombres y >35% en mujeres. En los tres años de seguimiento, los
pacientes con baja composición grasa tuvieron una mayor mortalidad en
forma independiente del IMC. El grupo con baja composición grasa y bajo
IMC asociado tuvo una mortalidad del 11% contra menos del 4% en los
otros tres grupos. El odds de aumento de riesgo fue 4,25 (IC
1,76-10.23). Es decir, cuatro veces mayor la chance de muerte en el
grupo más delgado y con menor proporción de composición grasa en el
peso. Evidentemente el problema de la paradoja no es explicable por el porcentaje de peso graso.
Explicación 3:
Luego del diagnóstico de enfermedad, los pacientes con exceso de peso
corrigen su riesgo con el tratamiento, aún sin cambiar su peso, en mayor
medida que los normales o delgados.
El aumento de peso se asocia al
desarrollo de hipertensión arterial, dislipemia y diabetes, y gran parte
del riesgo asociado se explica por estos factores. Una hipótesis que
podría explicar la mejor evolución alejada es que tanto la presión
arterial como la dislipemia hoy pueden ser controladas con la medicación
aún cuando no se modifique el peso corporal. Una observación de gran
valor en ese sentido fue aportada por la publicación de una gran cohorte
de pacientes en Holanda luego de una angioplastia coronaria7. En
primer instancia confirmaron en sus 6332 pacientes seguidos durante una
mediana de 6,1 años, una menor mortalidad evolutiva en los pacientes
con sobrepeso y obesos, 25 y 28% menor respectivamente que los pacientes
con peso “normal” confirmando las curvas que se habían reportado
anteriormente y graficamos en la figura 1.
La observación más interesante de este ensayo fue que el
tratamiento médico óptimo logrado fue superior en los obesos que en los
normales: 85% vs. 75% respectivamente. Definieron como tratamiento
óptimo al uso de por lo menos tres de las cuatro medicaciones probadas
que reducen la mortalidad alejada: aspirina, estatinas, beta bloqueantes
e inhibidores de la enzima convertidora. El cumplimiento del
tratamiento se asoció a mejor pronóstico, y en el análisis multivariado
mostró que al tomar en cuenta la adherencia, la asociación entre el
índice de masa corporal con el pronóstico dejaba de ser significativa.
Este estudio sugiere que la diferencia evolutiva entre los pacientes
obesos y normales luego de una angioplastia está mediada por el
cumplimiento de las medidas de tratamiento recomendadas, es decir, por
una conducta diferente en el cumplimiento de las pautas de prevención
secundaria.
Otra forma de pensar el tema en el mismo sentido es que la influencia de
la obesidad sobre el riesgo puede en gran medida ser frenada con el
control de la presión y el colesterol. En los pacientes más delgados,
podrían operar factores genéticos o no reconocidos que no se
modificarían, manteniendo su tendencia espontánea a nuevos eventos.
Explicación
4: La distribución de la grasa corporal tiene más importancia que su
magnitud absoluta, y contendría el verdadero mensaje de riesgo de la
obesidad.
La distribución de la grasa corporal se
relaciona con el riesgo cardiovascular en forma independiente del Índice
de masa corporal. La distribución de la grasa corporal “en manzana”
(mayor perímetro de cintura y mayor relación cintura cadera), denominada
obesidad andrógina, se asocia a mayor riesgo cardiovascular que la
distribución “en pera”. En esta última, con mayor perímetro de las
caderas y menor índice cintura cadera, denominada obesidad ginecoide, el
riesgo es mucho menor. En el estudio INTERHEART, se observó que el
incremento del índice cintura cadera (ICC) tenía una correlación más
fuerte con la presencia de infarto que el índice de masa corporal, y
discriminaba mejor los grupos de riesgo.8
En el estudio IDEA 9 se
efectuaron mediciones de perímetro de la cintura y del peso e Índice de
masa corporal en 160.000 personas que consultaron en atención primaria.
Observaron una correlación entre ambos parámetros y la presencia de
diabetes o enfermedad cardiovascular, con una mejor contribución del
perímetro de la cintura corregido por el IMC. Así, en pacientes sin
exceso de peso aparente, el aumento del perímetro abdominal se asoció a
diabetes y cardiopatías.
Obesidad visceral vs. obesidad subcutánea
Existen variadas hipótesis para explicar
este fenómeno, dada la compleja actividad metabólica y hormonal de los
adipocitos que es muy diferente en la grasa perivisceral que en la
subcutánea.
En una publicación fisiopatológica, Mc Carty10
sostiene haber resuelto la paradoja: la obesidad “periférica” (menos
abdomen, más caderas) tendría efecto por una serie de propiedades de
esos adipocitos (aumento de la actividad de la lipoprotein-lipasa,
diferentes niveles de producción de adiponectina, y así diferencias en
su efecto antiinflamatorio, sobre de la resistencia a la insulina y la
progresión de la aterosclerosis). La adiponectina, una hormona
producida por el tejido graso y con efectos beneficiosos
antiinflamatorios y antiaterogénicos, se reduce en la obesidad, pero
particularmente en la de distribución andrógina.11
Esta hipótesis se evaluó en un metaanálisis reciente. Los autores
investigaron el valor pronóstico luego de un evento coronario agudo del
índice de masa corporal y la denominada obesidad central tomando en
consideración el índice cintura cadera o el perímetro abdominal.
Incluyeron cuatro ensayos publicados y una serie de la Mayo Clinic.12
En un total de 15.923 pacientes, de los cuales pudieron obtener los
datos individuales de las bases de datos, en un seguimiento de una
mediana de 2,3 años, observaron que un mayor índice cintura cadera
corregido por el IMC se asoció a mayor mortalidad. Dividendo el índice
de cintura-cadera por tercilos, en el tercilo superior respecto del
inferior la mortalidad fue un 70% mayor en el grupo con IMC normal y 93%
mayor en el grupo de obesos. En este estudio, el índice de masa
corporal mantuvo su correlación negativa con la mortalidad.
El mensaje explícito de este estudio es que la obesidad central es un
factor de riesgo para mayor mortalidad, que explicaría en parte la
debilidad del índice de masa corporal respecto del índice cintura cadera
en su rol pronóstico.
¿Puede la diferencia entre abdomen prominente y caderas abultadas explicar la paradoja?
En lo personal creo que esta no puede ser la explicación de la paradoja de la obesidad por varios motivos lógicos
- La única forma de explicar la paradoja sería que a mayor
incremento del peso, aumentarían más el perímetro de las caderas que el
perímetro abdominal, y que justamente la grasa periférica ejercería un
efecto beneficioso. En el estudio, sin embargo, los pacientes con
mayores IMC, se asociaron con valores mayores del índice cintura cadera y
del perímetro de la cintura.
- Si existiera este efecto, las curvas evolutivas no tendrían
porqué ser diferentes en personas sanas que luego de un evento
cardiovascular.
- Los tercilos de perímetro cintura cadera en este trabajo no
fueron informados en forma no ajustada al índice de masa corporal. Dado
que a mayor peso crece más la cintura que la cadera en el promedio de la
población estudiada, es de suponer que en el análisis univariado el
perímetro no se asoció a mayor riesgo y me permito suponer que en
realidad tuvo el mismo comportamiento que el IMC: cuanto mayor perímetro
abdominal menor riesgo evolutivo sin efectuar un ajuste estadístico.
Su asociación con mayor riesgo sólo se hizo evidente al corregir por el
IMC. Para aclarar este punto: en las personas delgadas los criterios
para dividir tercilos de perímetro de cintura en varones fueron 84 y 90
cm. En los obesos, los puntos de corte de los tercilos fueron 107 y 115
cm. Tener más de 90 cm de perímetro de cintura si el IMC es normal tiene
mucho más riesgo que tener 107cm si el IMC es elevado. Es evidente que
no hay un valor común que ayude a estratificar por perímetro de cintura o
ICC, sino solo adquiere valor cuando se considera el IMC.
En un editorial13 con un título por demás expresivo: Exceso adiposo tisular/grasa ectópica: la clave faltante de la paradoja de la obesidad,
el autor defiende este concepto, pero aclara que no existe un valor de
perímetro abdominal o Índice cintura cadera que pueda ser considerado
con independencia del índice de masa corporal, es decir, del nivel de
peso corporal.
Explicación
5: la asociación entre obesidad, riesgo cardiovascular y mortalidad no
es similar en diferentes grupos etarios y de riesgo, y está mal
comprendida.
Hemos aceptado que en la población sana
el mayor peso se vincula al desarrollo de hipertensión, diabetes, y
enfermedad cardiovascular en edades más tempranas. Sin embargo la
influencia no es homogénea y puede variar en diferentes grupos etarios.
En la revisión clásica que resume la influencia del IMC sobre la
evolución alejada, en 900,000 personas adultas incluidas en estudios
prospectivos14, se confirma con
claridad que el menor riesgo de muerte está en 22 a 25 de IMC. En la
figura 3 se observa asimismo el comportamiento en J, con mayor riesgo de
muerte evolutiva en los delgados (<18 de IMC) y en los obesos, con
una pequeña diferencia en los excedidos en peso. Como ejemplo, se
requiere un IMC muy elevado, superior a 36 para equiparar el riesgo de
personas con peso bajo, IMC 16. Este comportamiento es similar en
mujeres, aunque con menor riesgo de muerte anual para cada categoría
respecto de los varones, y está ajustado por edad.
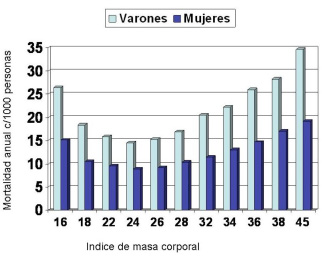
Riesgo
de muerte en adultos de acuerdo al índice de masa corporal ajustado por
edad, en cada sexo. Se observa un comportamiento en J o U, con el valle
de menor riesgo en el segmento de 22-24 de IMC. Los datos fueron
tomados del Prospective Studies Collaboration.
Tomando como óptimo 22,5 a 25 kg/m2 de IMC,
en adultos de mediana edad puede proyectarse que la sobrevida en las
personas con IMC 30 a 35 se reducirá en 2 a 4 años, y en el grupo de 40 a
45 de IMC en 8 a 10 años.
En el año 2010 se publicó un nuevo análisis que abarcó 1.460.000 adultos
con curvas muy similares. En forma global, el riesgo fue menor con IMC
de 22,5 a 25.15 Estos resultados se resumen en la figura 4.
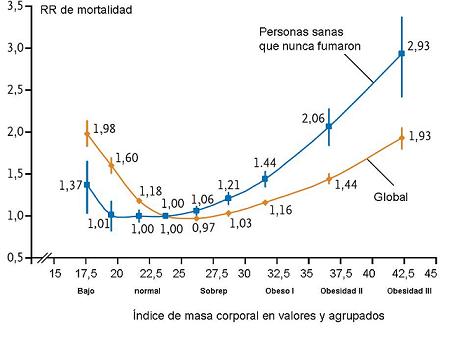
Figura 4
Relación
entre el IMC y la mortalidad evolutiva. Se observa que en la población
global existe poca diferencia de riesgo entre 22,4 y 32,5,
incrementándose el riesgo por encima de 35 de IMC, RR 1,44, o por debajo
de 20. 1,60. Si se considera la población no fumadora la curva es más
similar a la figura 3. (15).
Índice de masa corporal, edad avanzada y riesgo cardiovascular
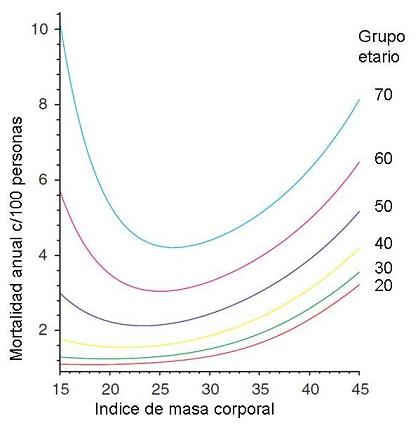
El nivel ideal de IMC se va modificando con la edad. En la figura 5,
observamos que con el incremento de la edad, el valle que indica menor
riesgo de mortalidad se va desplazando a IMC mayores, compatibles con
las categorías excedido en peso u obesidad I, respecto de los delgados e
incluso los denominados normales. 16
En series clásicas en personas mayores de 70 años el IMC ideal corregido
por una serie de variables se ubica en 30-32, es decir, en el nivel de
obesidad I 17. En una serie más reciente de 1008 personas mayores de 65 años en España seguidos por 11,6 años 18,
observaron que el IMC ideal se ubicada en el rango de 30 a 35, es
decir, obesidad grado I. La sobrevida promedio en los obesos grado I fue
de 13,8 años, en los excedidos en peso fue de 12,3 años, en los
normales 10 años y en los delgados 5,6 años. En este grupo etario, los obesos sobrevivieron en promedio casi cuatro años más que los “normales”.
Figura 5
Relación
entre la mortalidad expresada en muertes cada 100 personas, y el Índice
de masa corporal para diferentes grupos etarios. Se observa una
migración del nadir de riesgo de personas de mediana edad cercano a
22-25 hacia 28-30 de IMC en grupos más añosos. (16).
Las curvas de la relación entre
el IMC y la mortalidad en pacientes coronarios son prácticamente
idénticas a los grupos etarios mayores..
¿La paradoja de la obesidad modifica las recomendaciones dietéticas? Evidencias y dieta
Pocas semanas atrás me visitó un
paciente de 65 años que tiene colocado un stent farmacológico por una
lesión asintomática de la arteria descendente anterior cuatro años
atrás. Mide 1,78 y pesa 81 kg, tiene la presión normal, el colesterol
LDL muy bajo, no fuma y hace ejercicio. Vive atemorizado frente a un
eventual avance de la enfermedad que nunca le dio síntomas. Consultó un
colega que le recomendó bajar esos “3 kilitos”, lo que ha intentado
hacer en reiteradas oportunidades y le resultó difícil de lograr.
¿Existen evidencias para esta sugerencia? O quizás sería mejor preguntar
si existen evidencias de beneficio clínico de alguna dieta orientada a
la reducción de peso o hipograsa, o alguna modificación de peso
inducida por los médicos en pacientes coronarios que haya demostrado un
efecto beneficioso.
La respuesta es NO.
Dieta Hipograsa
Luego de un infarto por ejemplo, se sugiere a los pacientes una dieta
hipograsa, y tratar de bajar de peso si pertenece a los grupos de peso
excedido u obesos.
La dieta hipograsa ha sido evaluada prospectivamente en varios ensayos
con resultados sistemáticamente negativos. En un metaanálisis la
reducción relativa de riesgo fue 6% (IC -6 a +16%), no significativo.19 Posteriormente
se conoció el seguimiento a diez años del estudio de dieta DART . El
consejo de consumir menos grasa en la dieta tuvo poco efecto de
cumplimiento y no se asoció a reducción en la mortalidad. En el mismo
estudio el agregado de aceite de pescado se asoció a reducción
significativa de la mortalidad.
La dieta hipograsa en prevención primaria ha sido evaluada en un ensayo
de grandes dimensiones en mujeres . Incluyeron 48.835 mujeres
postmenopáusicas que ingerían más del 30% de las calorías como grasas
(en promedio 35%) y redujeron ese porcentaje a un promedio del 28%. El
estudio se prolongó por cinco años, con una elevada tasa de cumplimiento
en la dieta. En promedio el peso se redujo 1kg con la dieta hipograsa,
no se modificaron significativamente los niveles lipídicos, y no tuvo
ningún efecto sobre la morbimortalidad. La conclusión obvia del estudio
es que la recomendación actual en Estados Unidos de la proporción
deseable de calorías favoreciendo hidratos de carbono o proteínas
respecto de grasas aun cuando se cumpliera no ejerce efectos beneficiosos sobre la salud.
Lo poco que tenemos sobre recomendaciones de dieta basados
en evidencias se orienta al uso de dieta mediterránea, enriquecida en
aceite de oliva, frutas, nueces, que no tiene como objetivo la reducción
de peso.
Evidencias sobre bajar de peso
Estudios de reducción de peso en general
En las series que han controlado
pacientes en diferentes oportunidades por largos períodos, la pérdida
evolutiva del peso en forma general en ausencia de patologías aparentes
que las motiven, se asocia a mayor mortalidad evolutiva. Esta
disminución no distingue entre descensos intencionales o no.
Como ejemplo, un estudio efectuado en Malmo, Suecia, incluyó 5.722
personas sin patología aparente que fueron controlados cada 6 años en
dos oportunidades, comparando la evolución del IMC y la evolución
clínica ulterior durante 16 años. Excluyeron muertes por cáncer y las
muertes del primer año luego del segundo control para evitar factores de
confusión. Aquellos que disminuyeron en promedio su IMC en por lo menos
un punto en diez años (equivaldría a 4 kg en forma aproximada) tuvieron
un riesgo incrementado de mortalidad que de acuerdo al grupo de IMC
basal osciló de 1,4 a 2,6 veces, es decir, un 40 a 160%. También se
incrementó en aquellos que aumentaron su IMC si eran inicialmente
obesos. Considerando las personas no fumadoras, los obesos tuvieron una
mayor mortalidad cuando bajaron de peso que cuando se mantuvieron
estables. Para los investigadores, la pérdida de peso se asoció a mayor
riesgo evolutivo, lo que fue más pronunciado en obesos no fumadores.22
Otros estudios han confirmado la misma observación: la pérdida de peso
evolutiva o la fluctuación se asocian a mayor riesgo. Una cohorte de
8.479 del estudio NHANES-I 23 informó
que en los pacientes que tuvieron fluctuación del IMC el riesgo fue 83%
mayor (IC 25-170%). También se observó un riesgo multiplicado de
mortalidad cardiovascular RR 3,36 (IC 2,5 a 4,5) en los que descendieron
de peso, en comparación con el grupo de pacientes obesos estables.
Estas observaciones tienen un sesgo muy importante, dado que asocia en
el mismo grupo el descenso intencional de peso, vinculado a la intención
de prevención, con el descenso no intencionado vinculado a factores
poco conocidos o enfermedades subyacentes inaparentes.
Tiene un mayor interés evaluar el efecto del descenso de peso en quienes
lo intentan voluntariamente a través de diferentes medidas.
¿Qué ocurriría si los pacientes “hicieran caso” y bajaran de peso? Descenso intencional.
No tenemos una respuesta más que
especulativa a esta pregunta, pero en nuestra imaginación asumimos que
les iría mejor. Sobre la base de estudios de corto alcance podemos
esperar que resulte facilitado el control de la presión arterial, la
colesterolemia y la glucemia.
Carecemos de esta información en pacientes con coronariopatía, pero
existen varias series epidemiológicas que han evaluado el descenso
intencional del peso y la contribución de la pérdida de peso sobre el
riesgo de mortalidad.
En primera instancia, el resultado es diferente en personas que toman la
decisión de bajar de peso por su cuenta que en aquellos que lo hacen
por indicación médica. En una investigación en 4.896 individuos de 56 a
75 años se analizó la pérdida de peso no intencional o intencional, y en
ese caso la motivación.24 En
primera instancia confirmaron que el descenso no intencional se asoció a
un incremento del 71% de la mortalidad. En los que disminuyeron
intencionalmente de peso el comportamiento fue heterogéneo: en aquellos
que surgió como una decisión personal cayó el riesgo de muerte 41% a
expensas de enfermedades cardiovasculares. En los que bajaron de peso
por recomendación médica o por problemas definidos de salud, el riesgo
de mortalidad tendió a incrementarse un 37%.
En otra cohorte 25 de 2.957
participantes adultos sanos con IMC mayor a 25 kg/m2 se analizó la
intención de bajar de peso y su relación con la evolución alejada. En
ese grupo, los que descendieron de peso tuvieron incremento del riesgo
de muerte del 86% comparados con los que se mantuvieron estables e
incluso con los que aumentaron de peso. La conclusión de los autores es
que la pérdida de peso deliberada en los individuos con sobrepeso sin
comorbilidades puede ser peligrosa en la evolución alejada.
En un metaanálisis 26 de 26
ensayos que evaluaron el efecto de la intención de bajar de peso en
personas obesas sin patologías asociadas, el descenso de peso
intencional tuvo un efecto neutro sobre la mortalidad en forma global,
RR 1,01. La pérdida de peso no intencional se asoció a un incremento del
22 al 39% de riesgo. En individuos obesos considerados enfermos con
patologías relacionadas, la pérdida de peso tuvo un beneficio pequeño
sobre la mortalidad 16% (3 al 27%), pero en individuos son sobrepeso aún
con patologías asociadas la mortalidad se incremento 9% (2-17%). Como
vemos el eventual efecto beneficioso del descenso de peso voluntario es
en el mejor de los casos pequeño, con variaciones de acuerdo al grado de
IMC inicial, la presencia de patología y un comportamiento en subgrupos
poco convincente.
Efectos de la reducción de peso luego de un evento coronario
Prácticamente no hay ensayos que hayan evaluado la utilidad de bajar de
peso luego de un infarto con un suficiente número de pacientes que
permita obtener una conclusión. El problema radica en que no existe un
tratamiento eficaz para lograr reducción de peso de cierta magnitud,
salvo la cirugía bariátrica.
En la última década se planificaron dos ensayos de grandes dimensiones
con intervenciones dietéticas; uno predominantemente en pacientes con
antecedentes cardiovasculares y otro en diabéticos.
El estudio SCOUT incluyó 10.744 personas con antecedentes
cardiovasculares (68%) y /ó diabetes, con un índice de masa corporal
entre 27 y 45 kg/m2. El promedio de IMC fue 33, el perímetro medio de
cintura 114 cm en hombres y 109 cm en mujeres, y el peso promedio 97 kg.
Todos los pacientes fueron tratados con dieta y controles, y uno de los
dos grupos recibió sibutramina. El descenso de peso promedio en el
seguimiento fue de 1,9 kg en el grupo placebo y 4,3 kg con sibutramina.
La diferencia a favor de la droga fue de 2,4 kg promedio con un
seguimiento de 3,4 años. A pesar de la reducción de peso la sibutramina
se asoció a aumento de las pulsaciones (3 latidos promedio), de la
presión arterial, 1mmHg, y a incremento del riesgo de infarto y ACV no
fatal, lo que llevó a la suspensión del estudio. No hubo diferencias en
la mortalidad global o cardiovascular.
Este estudio muestra también los límites de nuestras intervenciones
actuales para reducir el peso. Carecemos de drogas validadas con
excepción del orlistat. La intervención dietética en un ensayo con
múltiples controles indujo en el grupo sin fármacos sólo 1,7 kg de
reducción del peso. La mayor reducción obtenida con sibutramina, en el
rango de lo mejor que puede obtenerse con dieta en estudios controlados,
no tuvo impacto beneficioso sino dañino, quizá antagonizado por sus
efectos adversos cardiovasculares aunque estos fueron muy modestos.
El otro estudio Look Ahead Trial28
incluyó prospectivamente 5.145 pacientes, 59,5% mujeres con una edad
promedio de 58,7 años, con diabetes tipo II y excedidos en peso u
obesos. Se comparó el tratamiento habitual con recomendaciones
dietéticas y fármacos, con una intervención múltiple con ejercicios
frecuentes, reuniones grupales, provisión de dietas y controles más
frecuentes. El estudio está diseñado para un seguimiento a 13 años, y se
han conocido los primeros resultados a cuatro años. La intervención
múltiple se asoció a reducción de peso (6% del peso corporal vs. 1% en
el grupo control), mejor capacidad aeróbica, y disminución de la presión
sistólica 2,3 mmHg, diastólica 0,5 mmHg, y de los niveles de
hemoglobina glicosilada (0,36% vs. 0,09% en el grupo control).
Curiosamente, los niveles de colesterol LDL fueron más bajos en el grupo
control, por el uso de mayores dosis de estatinas. Estos efectos no se
reflejaron en la evolución clínica en los primeros cuatro años y deberá
esperarse la evolución alejada para estimar el beneficio eventual.
El efecto del peso sobre la evolución será complejo de aislar de otras
variables como el entrenamiento aeróbico, que es mayor en el grupo de
intervención múltiple. En pacientes con enfermedad coronaria la utilidad
de la rehabilitación cardiovascular está bien consolidada con
reducciones del 20% de la mortalidad total y del 27% de la mortalidad
cardiovascular.
Comentario final: Recomendaciones dietéticas y evidencias
Tenemos pocas herramientas útiles para apoyar nuestra
estrategia orientada a la reducción del peso, y lo que es peor, ni
siquiera podemos afirmar que si lo lográramos tendríamos algún
beneficio. Es imposible imaginar que bajar de peso se logre sin
ningún precio en modificaciones conductuales, farmacológicas, de estilos
de vida, cuya resultante final debería ser evaluada en ensayos de
grandes dimensiones.
Las evidencias poblacionales indican que en la mayoría de los
pacientes que atiende un cardiólogo, es decir, población añosa o con
enfermedad cardiovascular conocida, los excedidos en peso y obesos I no
tienen en el peor de los casos un mayor riesgo que los normales y
siempre menor riesgo que los delgados. Hemos discutido lo difícil que es
extraer una conclusión práctica de esta observación, que tiene
interpretaciones múltiples y conflictivas. Pero lo que no cabe duda es
que disminuye nuestra convicción sobre el modelo de interpretar el peso
corporal “ideal” y su relación con el pronóstico en pacientes
coronarios.
Tratando de proyectar esta voluminosa información epidemiológica,
clínica y fisiopatológica a la práctica del consultorio, quizá la
conclusión sea sencilla.
En prevención secundaria, tenemos evidencias indudables del beneficio
sobre la mortalidad de intervenciones farmacológicas (aspirina,
estatinas, beta bloqueantes, inhibidores de la enzima convertidora en
particular en presencia de disfunción ventricular), y no farmacológicas
como el ejercicio en programas de rehabilitación.
No tenemos en este contexto ninguna evidencia clínica de los beneficios
de bajar los contenidos grasos de la dieta o intentar bajar de peso en
ninguno de los grupos de IMC. Incluso algunas observaciones
epidemiológicas se orientan en sentido contrario.
Creo que con toda humildad debemos transmitir esta información a los
pacientes que nos consultan: no sabemos si bajar de peso mejorará su
pronóstico clínico ni cómo lograrlo, no sabemos si comer menos grasas
tiene alguna utilidad, y lo poco que sabemos sugiere migrar a una dieta
tipo mediterránea, es decir, más pescado, frutas, nueces y aceite de
oliva. En contextos particulares, como casos de difícil control de los
parámetros con estrategias farmacológicas (hipertensión, dislipemia,
glucemia) el bajar de peso es ya una indicación terapéutica con un
objetivo preciso, y justifica el inmenso esfuerzo y cambio cultural
requerido.
Quizá las recomendaciones que seguimos repitiendo sin sentido tienen su
raíz en planos menos científicos. No debemos olvidar que obeso tiene su
origen etimológico en “comer mucho”, y que la gula ha sido considerada
un pecado capital. La obesidad no se ha desligado de su estigma de
comportamiento pecaminoso, un fracaso personal al no poder reprimir
pasiones nocivas, una conducta que merece algún castigo, y algo de eso
sigue incluido en el discurso irreflexivo de la importancia de bajar
“los 3 kilitos que tiene de más”.
 * Dr. Carlos Tajer: Médico cardiólogo, experto en metodología de la investigación, autor de numerosos trabajos de la especialidad, del libro"Evidencias en Cardiología" y del libro "El corazón Enfermo", de la editorial Libros del Zorzal. Docente de los cursos de GEDIC , director de la revista de la Sociedad Argentina de Cardiología.
* Dr. Carlos Tajer: Médico cardiólogo, experto en metodología de la investigación, autor de numerosos trabajos de la especialidad, del libro"Evidencias en Cardiología" y del libro "El corazón Enfermo", de la editorial Libros del Zorzal. Docente de los cursos de GEDIC , director de la revista de la Sociedad Argentina de Cardiología.
*
IntraMed agradece al Dr. Carlos Tajer y a la revista de la Sociedad
Argentina de Cardiología la generosidad de compartir su trabajo con
nuestros lectores.
Fuente: intramed















 * Dr. Carlos Tajer: Médico cardiólogo, experto en metodología de la investigación, autor de numerosos trabajos de la especialidad, del libro
* Dr. Carlos Tajer: Médico cardiólogo, experto en metodología de la investigación, autor de numerosos trabajos de la especialidad, del libro